Sida 1 av 2
Tid: 75 minuter
- Tillåtna hjälpmedel är penna, suddgummi och linjal, formelsamling, samt miniräknare.
- Alla svar ska skrivas på ett annat papper. Detta papper kan du behålla om du vill.
- Alla reaktionsformler skall vara balanserade med minsta möjliga heltalskoefficienter.
- Antalet poäng per uppgift ges på formen (G/VG/MVG). Exempel: Intill en fråga står det ”(1/1/0)”. Det betyder att man kan få maximalt 1 G-poäng och 1 VG-poäng.
Del I. Endast svar behöver anges. Glöm inte enhet!
- I ett lufttätt kärl har jämvikten
N2O4(g)
⇌
2NO2(g)
∆H > 0 för reaktionen åt höger
färglös rödbrun
fått ställa in sig. Dikvävetetraoxiden, N2O4, är färglös, medan kvävedioxiden, NO2, är rödbrun.- Ställ upp jämviktsekvationen för reaktionen. (1/0/0)
- Vad händer med gasblandningens färg om man tillsätter mer N2O4? (1/0/0)
- Vad händer med gasblandningens färg om man ökar trycket i kärlet? (0/1/0)
- Vad händer med gasblandningens färg om man minskar temperaturen på reaktionsblandningen? (0/1/0)
- Vilket pH har en lösning
- som består av 0,250 mol/dm3 salpetersyra, HNO3? (1/0/0)
- där [OH–] = 0,025 mol/dm3? (0/1/0)
- Vid 45 °C är vattnets jonprodukt Kw = 4,0·10-14 M2. Vilket pH har rent vatten vid 45 °C? (0/1/0)
- 2,0
- 6,7
- 7,0
- 7,3
- 13,4
- 14,0
Del II. Fullständiga lösningar ska redovisas. Glöm inte enhet!
- Vid 700 °C mätte man halten SO3, NO, SO2 och NO2 i ett lufttätt reaktionskärl där följande jämvikt ställt in sig:
SO2(g) + NO2(g) ⇌ SO3(g) + NO(g)
De värden man fick var: [SO2] = 0,12 M; [NO2] = 0,18 M; [SO3] = 0,32 M; [NO] = 0,11 M. Vilket värde hade jämviktskonstanten K? (1/0/0) - Man löser lite dinatriumvätefosfat, Na2HPO4 i vatten. Vilken reaktion får lösningen: Sur, neutral eller basisk? Motivera ditt svar. (1/1/0)
- Vid 25 °C är jämviktskonstanten K = 0,46 för nedanstående reaktion:
2BrCl ⇌ Br2 + Cl2
Vid ett visst tillfälle är [BrCl] = 0,30 M; [Br2] = 0,15 M och [Cl2] = 0,15 M.- Visa att systemet inte är i jämvikt (1/0/0)
- Åt vilket håll kommer reaktionen att gå? Motivera ditt svar! (1/1/0)
- Du tillverkar en buffert genom att blanda 25,0 ml 0,100 M NH3 med 75,0 ml 0,250 M NH4Cl. Beräkna buffertens pH. (1/1/0)
- Du har 0,250 dm3 av en lösning med 1,50 M ättiksyra. Vilket är lösningens pH? (2/2/0)
- Polyakrylamid, [-CH2-CH(C(O)NH2)-]n, är en polymer av akrylamid, CH2CHC(O)NH2. Det betyder att polyakrylamid är ett stort ämne som är uppbyggt av många små akrylamid-rester. Polyakrylamid är helt ofarligt, medan akrylamid är giftigt och kan skada nervsystemet allvarligt.
När man tillverkar polyakrylamid kan det göras enligt följande kemiska reaktionsformel:
nCH2CHC(O)NH2 ⇌ [-CH2-CH(C(O)NH2)-]n
Eller, med strukturformler:
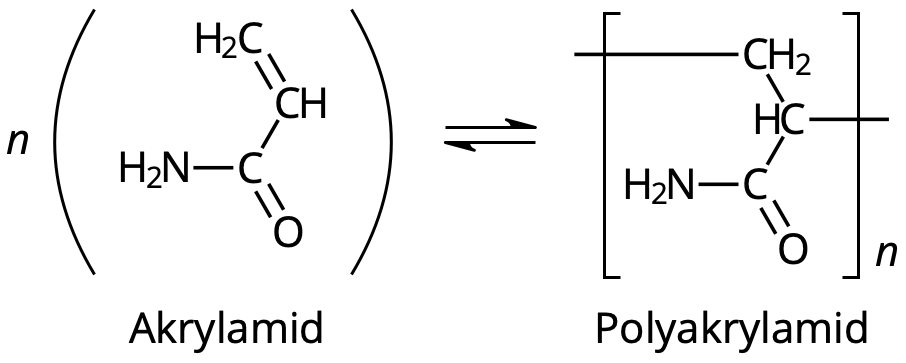
Reaktionen är en jämvikt som är starkt förskjuten åt höger.
Det kan vara en riktigt dum idé att försöka täta väggarna i tunneln genom Hallandsåsen med polyakrylamid. Använd både kemiska argument, beräkningar och ekologiska argument för att förklara varför! (2/2/2)
