Några begrepp
- Enzym = protein som katalyserar en viss reaktion.
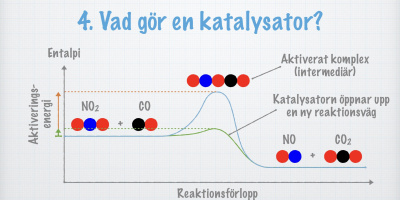
- Katalysator = ett ämne som påskyndar en reaktion utan att själv förbrukas.
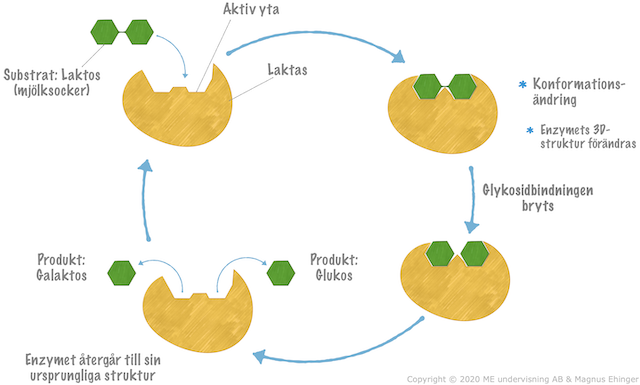
- Substrat = de eller det ämne som omvandlas med hjälp av enzymet.
- Aktiv yta = det ställe i enzymet, där substratet binder in.
- Produkt = det som bildas i reaktionen.
Varför ett enzym fungerar: Lite termodynamik
Allt i en enzymkatalyserad reaktion är jämviktsreaktioner!
Substrat ⇌ Produkt(er)
Vi kan teckna en jämviktskonstant för reaktionen:
\(K = \frac {\text{[Produkt(er)]}}{\text{[Substrat]}}\)
Kommer du ihåg: Vad är det enda som påverkar värdet på K?
- Temperaturen!
- Närvaron av ett enzym påverkar inte K.
- Närvaron av ett enzym påverkar endast reaktionshastigheten – så att jämvikten uppnås mycket, mycket snabbare.
Enzymer sänker aktiveringsenergin för en viss reaktion
Hur går det då till när ett enzym katalyserar "sin" reaktion?
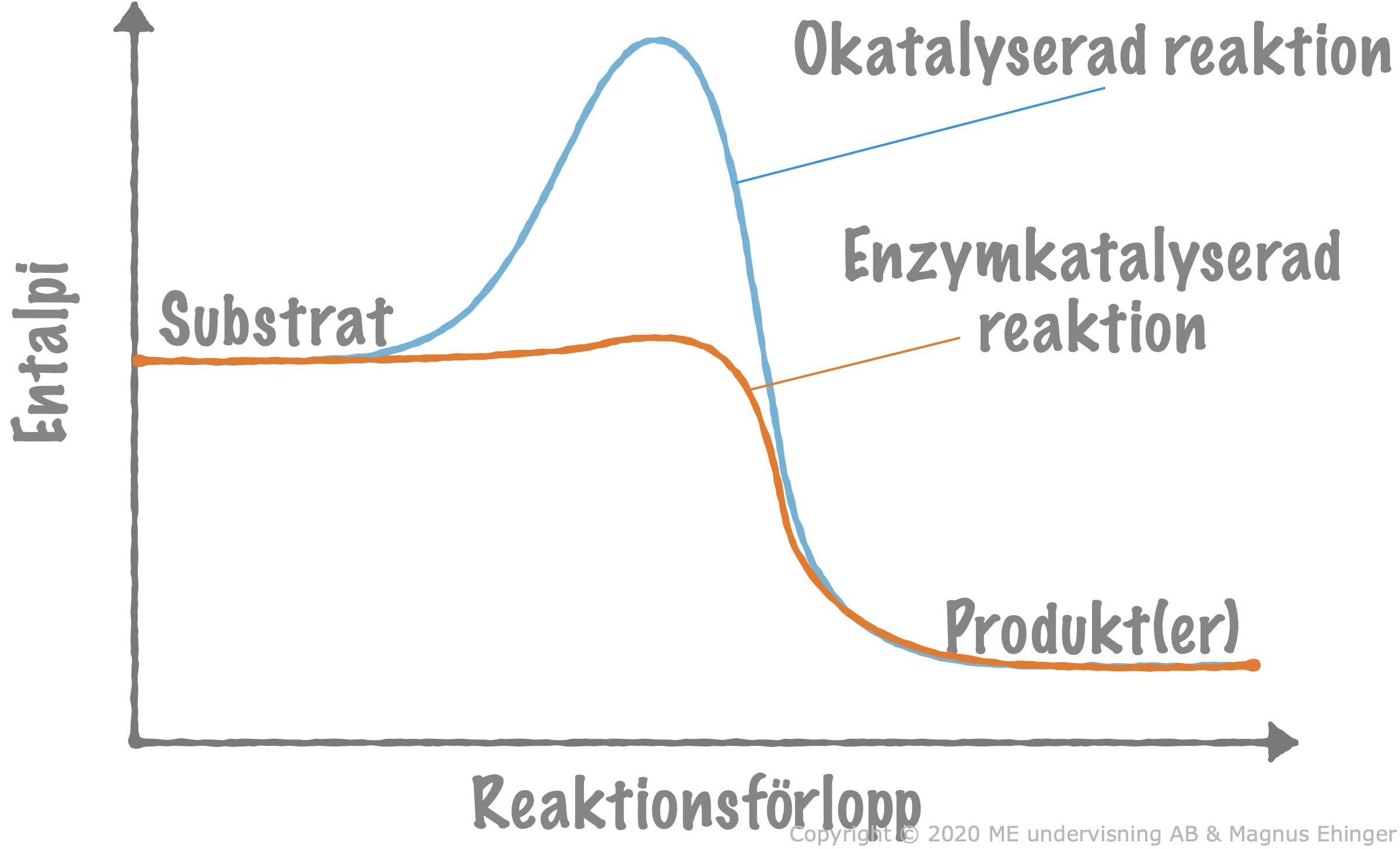
- Vi kan konstatera att jämviktstillståndet uppnås mycket snabbare med enzym än utan.
- Det beror på att enzymet sänker reaktionens aktiveringsenergi, d.v.s. den energi som krävs för att reaktionen ska kunna ske.
Hur kan ett enzym sänka aktiveringsenergin?
Kommer du ihåg: Vad händer (ur energisynpunkt) när det uppstår bindningar?
- Det frigörs energi!
När substratet binder till enzymet i steg 2 ovan, frigörs energi. Energin används till att bryta bindningen i laktos-molekylen.
Varför ett enzym inte fungerar: Inhibitorer
Om ett enzym fungerar eller inte beror helt och hållet på dess struktur. Därför är det lätt att tänka sig en bromskloss som på något sätt förhindrar att enzymet kan utföra sin uppgift.
Inhibitorer är molekyler som på något sätt binder till enzymet, och förhindrar att det sker någon reaktion.
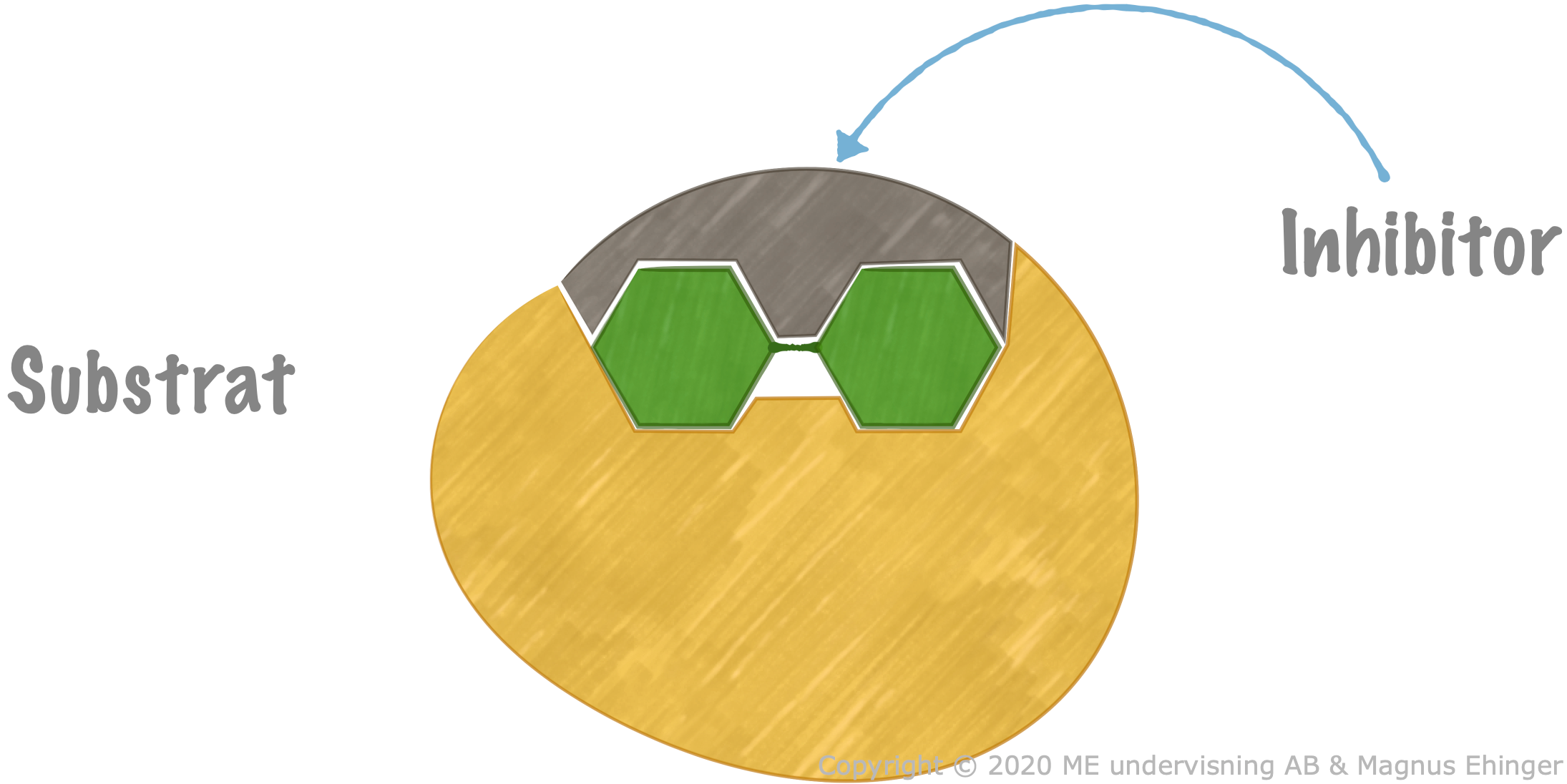
Kompetitiv inhibering
Kommer av engelskans compete = tävla. Både inhibitorn och substratet "tävlar" om att binda till enzymets aktiva yta. Om inhibitorn hinner först ("vinner tävlingen"), sitter den helt enkelt i vägen för substratet, och därför sker det ingen reaktion.
Icke-kompetitiv och anti-kompetitiv inhibering
Vid icke-kompetitiv inhibering binder inhibitorn inte till enzymets aktiva yta, utan någon annanstans på enzymet.
Att inhibitorn binder till enzymet leder ändå till en av två saker. Antingen
- enzymet ändrar form ⇒ substratet kan inte binda till den aktiva ytan ⇒ enzymet tappar sin funktion ⇒ ingen reaktion sker; eller
- inhibitorn förhindrar att enzymet ändrar form, även om substratet kan binda in ⇒ ingen reaktion sker.
Vid anti-kompetitiv inhibering har substratet redan bundit till enzymets aktiva yta, men innan det hinner ske någon reaktion binder också en inhibitor till enzymet, och förhindrar att det sker någon reaktion.